Kvant hisoblashlari va Myobius molekulasi uchrashuvi

O'tgan hafta IBM o'zining g'ayrioddiy ilmiy ishiga qo'shgan hissasini e'lon qildi: kvant kompyuterida qisman ishlaydigan algoritm yordamida yarim-Möbius topologiyasiga ega molekula yaratish. Ochig'ini aytganda, bu maqolada juda ko'p ma'lumot bor edi va uni hazm qilish biroz vaqt talab qildi. Ammo u so'nggi bir necha o'n yilliklarda ishlab chiqilgan vositalar bilan qanday kimyo yaratishimiz mumkinligi, shuningdek, kvant hisoblashlari foydalilikka qanday qadam tashlayotgani haqida juda qiziq ma'lumot beradi.
Ammo to'liq tasvirni olish uchun uch xil hikoya kerak bo'ladi, shuning uchun biz katta rasmni birlashtirishdan oldin ularning har birini alohida ko'rib chiqamiz.
Burma orbitalar
O'rta maktab kimyo darslarini hali ham eslay oladiganlar, ehtimol, oltita uglerod halqasidan iborat, bir va ikki bog'lanishlar navbatlanib joylashgan, barcha uglerodlarni yassi molekula hosil qilib, bitta tekislikda ushlab turadigan benzolni eslashadi. Siz eslamasligingiz ehtimoli kamroq bo'lgan narsa shundaki, ikki bog'lanish uglerod atomlarining yadrosidan vertikal ravishda yuqorida va pastda joylashgan orbitalar orqali amalga oshiriladi. Bog'lanishlarning bir-ikki navbatlanish xususiyati tufayli bu orbitalardagi elektronlar delokalizatsiyalanadi; bog'lanishlar orasidagi farqlar biroz ahamiyatsiz bo'lib qoladi va molekula o'z elektronlarining bir qismi bulutda suzib yurganidek tasavvur qilinadi. Xuddi shunday bog'lanish tartibiga ega bo'lgan kattaroq molekulalar uchun ham xuddi shu narsa amal qiladi.
Benzoldagi orbitalarning joylashuvi shundayki, molekula atrofida aylanadigan har qanday elektron boshlangan joyiga qaytadi. Boshqa atomlarni uglerod halqasiga bog'lash orqali orbitalarni vertikaldan turli burchaklarga joylashtirish mumkin. Qo'shimcha orbitalarning to'g'ri kombinatsiyasi bilan narsalarni shunday burish mumkinki, elektron molekulaning tepasida boshlanadi (halqa yuzaga yassi yotgan deb hisoblasak), ammo halqa atrofida to'liq aylanishni tugatgandan so'ng pastga tushadi. U boshlangan joyiga qaytish uchun halqa atrofida ikkinchi aylanishni amalga oshirishi kerak bo'ladi.
Bu Möbius lentasi yuzasi bo'ylab yo'l izlashga bevosita o'xshaydi, u yerda ham boshlangan joyingizga qaytish uchun ikkita aylanishni amalga oshirishingiz kerak. Darhaqiqat, ba'zi oddiy Möbius molekulalari ilgari sintez qilingan.
Yangi tadqiqotni ajratib turadigan narsa shundaki, orbitalar va bog'lanishlar uchun oddiy benzol hosilalarida ko'rganimizdan ko'ra ko'proq imkoniyatlar mavjud. Katta, xalqaro jamoa (akademiklar va IBM tadqiqotchilari ham kiradi) yarim-Möbius joylashuvini yaratish yo'lini topdi, bunda halqa shaklidagi molekula orbitalari shunday joylashganki, molekula atrofida bitta aylanishdan so'ng elektron molekulaning na tepasida, na pastida, balki periferiya atrofida joylashgan bo'ladi.
U faqat pastga tushish uchun ikki marta aylanishi kerak edi. Va keyin boshlangan joyiga qaytish uchun yana ikki marta aylanishi kerak edi.
Bu barqaror konfiguratsiya emas; o'z holiga qoldirilsa, molekula qisqa vaqt ichida ancha oddiy konfiguratsiyaga aylanadi. Va uning aniq bir foydasi yo'q, hatto biz uni ilovalarni sinab ko'rish uchun yetarli darajada barqaror saqlay olsak ham. Ammo bu molekulyar darajadagi orbital konfiguratsiyalarni manipulyatsiya qilish qobiliyatimizni qiziqarli o'rganishdir va bu qobiliyat oxir-oqibat qanday foyda keltirishi noma'lum.
Kvant hisoblash kabi, u ham g'alati va murakkab
Agar siz shunchalik g'alati narsa yaratmoqchi bo'lsangiz, buni qanday qilish kerakligi aniq emas. Agar orbital konfiguratsiyalarni o'zgartirish oson bo'lsa, kimdir buni allaqachon qilgan bo'lardi. Va, bu ishni ta'riflovchi maqola mualliflari ta'kidlaganidek, kvant mexanikasi tomonidan ruxsat berilgan ko'plab potentsial orbital shakllar mavjud, ammo molekulada qo'llaniladigan aniq konfiguratsiya qaysi orbitalarning qancha elektronlar bilan band qilinganiga bog'liq bo'lishi mumkin.
Ammo kattaroq molekulalar bilan ishlaganda – bu yerda jamoa ikki xlor atomi bilan bezatilgan 13 uglerod halqasi bilan ishladi – ishtirok etadigan elektronlar soni murakkablashadi va ular orbitalarga nima qilishini hisoblash tobora qiyinlashadi. Bu holatda, siz uglerod atomlaridan 24 elektron, shuningdek, ikki xlor atomidan yana sakkiz elektron bilan band bo'ladigan orbitalar qatorini ko'rib chiqasiz. Bu orbitalar qanday ko'rinishi kerakligini aniq klassik simulyatsiyalarini bajarish qobiliyatimizdan tashqarida.
Ammo orbitalar kvant tizimidir va ularning tabiatini biz manipulyatsiya qila oladigan kvant tizimiga – kvant kompyuteriga moslashtirish mumkin. Aniq yechim mavjud kvant kompyuterlarining imkoniyatlaridan tashqarida bo'lsa-da, ular Namuna asosidagi kvant diagonalizatsiyasi deb nomlanuvchi aralash klassik-kvant algoritmning bajarilishida foydali ekanligini isbotladi.
Namuna olish algoritmi aynan shuni anglatadi: siz tizimning xatti-harakatlari bo'yicha ko'plab namunalar to'playsiz va ulardan uning xatti-harakatlari haqida umumiy qoidalarni chiqarish uchun foydalanasiz. Bu holatda, algoritmning klassik qismi kvant uskunasida bir nechta operatsiyalarni sozlashga yordam beradi, ularning har biri individual namuna beradi. Bu namunalar har birini klassik uskunaga qaraganda tezroq bajarish mumkin va u kvant uskunasining xato chegaralariga odatda duch kelmaydigan darajada qisqa. Kvant uskunasi tezligi tufayli ko'plab namunalar bajarilishi mumkin, shuning uchun har qanday individual xatolar muntazam natijalar bilan yopilib ketishi kerak.
Natijada, jamoa ma'lum manipulyatsiyalar to'g'ri boshlang'ich kimyoviy modda bilan yarim-Möbius molekulasini yaratishga yordam berishi mumkinligini tasdiqladi.
Buni qanday yaratasiz?
Ular yaratishga qaror qilgan molekula, yumshoq qilib aytganda, g'alati. Bu halqaning qarama-qarshi tomonlariga bog'langan xlorlar bilan 13 uglerod halqasi. Uglerodlarning toq soni borligi sababli, bu xlorlar halqaning bir tomonida beshta uglerod va ikkinchi tomonida oltita uglerodni o'rab turishini anglatadi (quyidagi tuzilmalarni ko'ring). O'z holiga qoldirilsa, molekula bir va uch bog'lanishlarni navbatma-navbat hosil qiladi. Ammo xlorlarning mavjudligi va toq sondagi atomlar bu navbatlanishni buzadi, bu esa ikki bog'lanish va bir nechta juftlanmagan elektronlarning paydo bo'lishiga olib keladi.
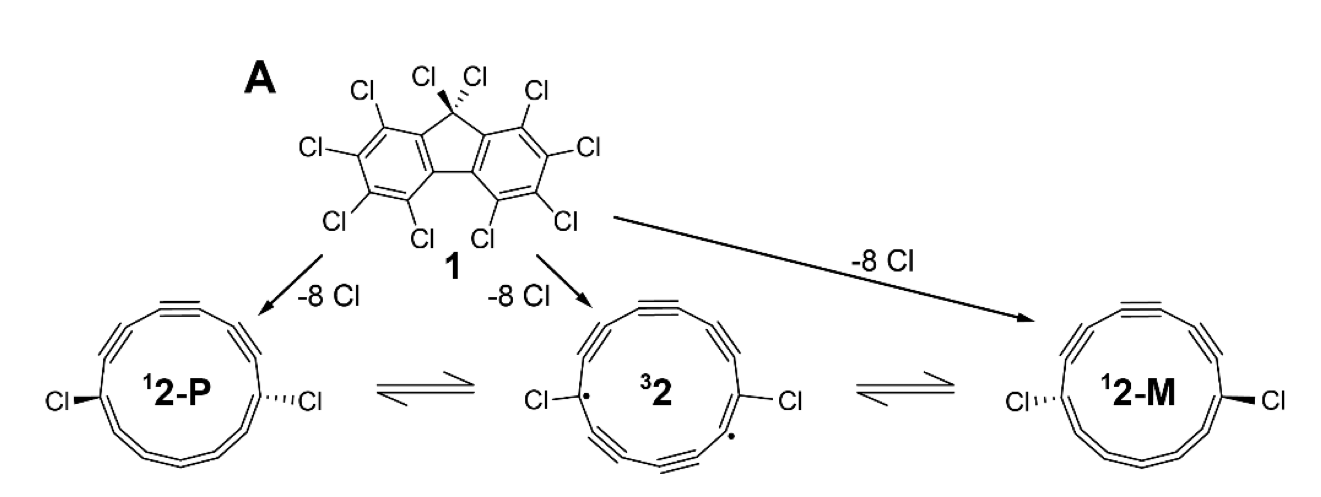
To'g'ri ishlov berish bilan boshlang'ich molekula (yuqoridagi) markaziy tuzilmani hosil qiladi. Voltajlarning yo'naltirilgan qo'llanilishi uni pastki qatordagi uchta shakl orasida o'zgartirishi mumkin.
Bularning barchasining bir natijasi shundaki, molekula haqiqatan ham barqaror emas. Tadqiqotchilar uni izolyatsiya qilingan holda, juda past haroratda va tuz kristalli yuzasida joylashgan holda saqlashdi. Ikkinchisi shundaki, uni sintez qila oladigan kimyoviy reaksiyalar ketma-ketligini loyihalash deyarli imkonsiz. Buning o'rniga, tadqiqotchilar ko'p xlorlar biriktirilgan uch halqali molekula bilan boshlashdi va skanerlovchi tunnel mikroskopi yordamida ma'lum atomlarga aniq voltajlar qo'llashdi, bir nechta uglerod-uglerod bog'lanishlarini uzishdi va xlor atomlarining ko'pchiligini ajratib olishdi.
To'g'ri molekula hosil bo'lgach, avvalgi simulyatsiyalar yordamida xuddi shu mikroskop molekulaga nisbatan aniq joylarga voltajlar qo'llash uchun ishlatildi. Bu molekulaning konfiguratsiyasini o'zgartirdi, ikki xlor atomini uglerod halqasi bilan belgilangan yassi tekislikdan chiqarib yubordi. Elektronlar shunday siljishdi-ki, xlorlar orasida beshta uglerod bo'lgan molekula tomonida bir qator ikki bog'lanishlar hosil bo'ldi; boshqa tomonda esa bir va uch bog'lanishlar ustunlik qildi.
Bu o'z navbatida, tadqiqotchilar maqsad qilgan yarim-Möbius konfiguratsiyasiga erishish uchun orbitalarning konfiguratsiyasini o'zgartirdi. Bu atom kuch mikroskopiyasi orqali tasdiqlandi, u orbital konfiguratsiyalarni qayd etdi va ular hisoblash namunalaridan olingan bashoratlarga asosan mos kelishini ko'rsatdi.
Buning ma'nosi nima?
Avvalo, bu yerda qilingan ishni qadrlash kerak, chunki buning ko'p jihatlari bir necha o'n yillar oldin fantastika deb hisoblanishi mumkin edi. Kimyoviy reaksiyalar orqali sintez qilish imkonsiz bo'lgan molekula oldida biz individual atomlarga aniq voltajlar qo'lladik va yagona molekulani o'zimizning aniq ehtiyojlarimizga moslashtirdik. Va keyin biz uning aniq bog'lanish konfiguratsiyasini qo'shimcha ravishda ehtiyotkorlik bilan qo'llanilgan voltajlar yordamida manipulyatsiya qildik.
Bularning barchasi molekulyar orbitalarning kvant mexanik xatti-harakatlari haqidagi ajoyib tushunchamiz tufayli amalga oshirildi.
Aksincha, kvant hisoblashdan foydalanish nisbatan oddiy tuyulishi mumkin. U aralash kvant/klassik algoritm bo'lib, xato stavkalari va kubitlar soni cheklovlarini chetlab o'tish uchun maxsus sozlandi (u IBMning Heron protsessoridagi 150 ga yaqin kubitning yarmidan ko'pini ishlatgan). Ammo bu keyingi bir necha yil davomida kvant hisoblashlari qanday ko'rinishi mumkin, chunki bizning asta-sekin kengayib borayotgan imkoniyatlarimiz har bir o'sish bilan bir nechta murakkabroq algoritmlarni qo'lga kiritishni boshlaydi. Va bu o'ziga xos tarzda juda hayajonli.
Science, 2026. DOI: 10.1126/science.aea3321 (DOI haqida).





